Banebrydende behandlinger forvandler plejen af atopisk dermatitis i 2026
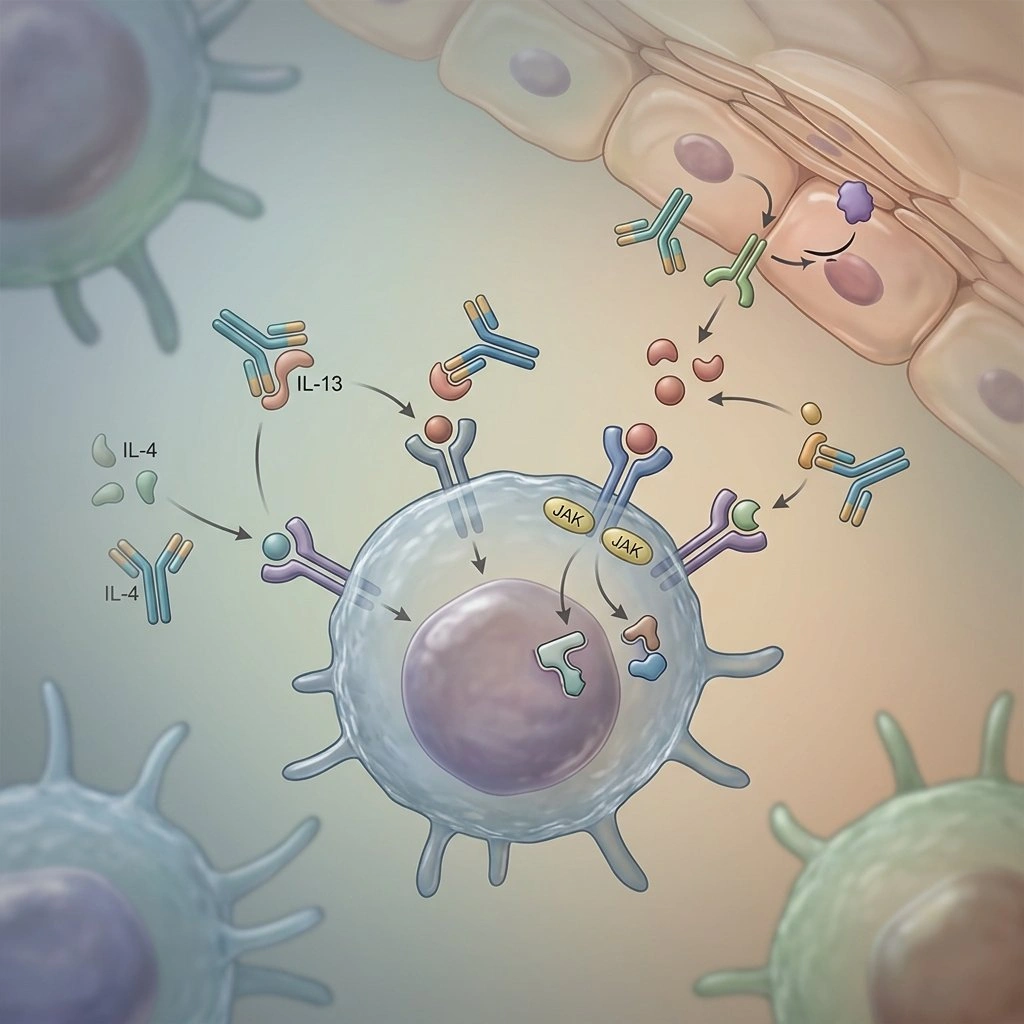
En ny æra: målrettede lægemidler ændrer, hvordan vi behandler atopisk dermatitis
Over de seneste år er behandlingen af atopisk dermatitis (AD) gået fra en værktøjskasse domineret af brede antiinflammatoriske lægemidler til en, der inkluderer højt målrettede muligheder—biologiske monoklonale antistoffer, orale Janus kinase (JAK) hæmmere og nye ikke-steroide topiske midler.
Denne nyere valgmuligheder er ikke bare ekstra muligheder; de har omformet beslutningstagningen i klinikkerne. Kliniske specialister overvejer nu tidligere brug af målrettede midler i stedet for at reservere dem som sidste behandlingsmuligheder, fordi mange af disse lægemidler tilbyder vedvarende sygdomskontrol med mekanismer, der er rettet mod den specifikke biologi, der driver en patients eksem (Kilde: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Hvordan specialister tænker på behandlingsrækkefølge
Førende klinikere ved en nylig specialkonference beskrev et klart skift i praksis: målrettede terapier er i stigende grad rygraden i langvarig behandling, mens traditionelle midler—som topiske kortikosteroider og topiske calcineurinhæmmere—ofte bruges som kortvarige broer eller til fokale udbrud.
Dette skift afspejler en voksende tillid til sikkerhedsprofilerne og varige reaktioner fra målrettede lægemidler og et ønske om at undgå langvarig, uspecifik immunsuppression, når det er muligt (Kilde: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Hvad “målrettet” betyder i hverdagspleje
Når dermatologer siger “målrettet,” mener de terapier, der afbryder en defineret immunvej, som er kendt for at drive AD-symptomer—så i stedet for at dæmpe immunaktiviteten bredt, blokerer disse lægemidler specifikke cytokiner eller signalmolekyler. Dette kan oversættes til bedre kløekontrol, forbedret søvn og klarere hud for mange patienter.
Eksempler, der har ændret praksis, inkluderer det anti-IL-4/IL-13 monoklonale antistof dupilumab og orale JAK-hæmmere som abrocitinib og upadacitinib, som alle er blevet almindelige muligheder for moderat til svær sygdom (Kilde: Regeneron Pharmaceuticals; Pfizer; AbbVie pressemeddelelser).
Et udvidende terapeutisk landskab: hvad der er tilgængeligt nu
Omfanget af godkendte og undersøgte muligheder er hurtigt blevet bredere, hvilket giver klinikere og patienter flere måder at matche behandling til individuelle behov.
Topiske, ikke-steroide lægemidler—som tapinarof, topisk ruxolitinib og roflumilast—har givet klinikere alternativer til langvarig topisk kontrol, især når det er ønskeligt at minimere steroideksponering (Kilde: Dermavant/Incyte/Arcutis pressemeddelelser).
På det systemiske område giver orale JAK-hæmmere (for eksempel abrocitinib og upadacitinib) og flere biologiske monoklonale antistoffer (herunder dupilumab, tralokinumab, lebrikizumab og nemolizumab) højt målrettede muligheder for patienter med udbredt, refraktær eller svær sygdom (Kilde: Pfizer; AbbVie; Regeneron; LEO Pharma; Eli Lilly; virksomhedens pressemeddelelser).
Fra for få muligheder til for mange valg
Selvom det er gode nyheder at have flere behandlinger, har det ændret den kliniske udfordring: læger står nu over for komplekse beslutninger om, hvilken terapi der skal startes, hvornår der skal skiftes, og hvordan behandlingerne skal sekventeres for det bedste langsigtede resultat.
Denne kompleksitet kræver omhyggelig evaluering af sygdomsfunktioner, sikkerhedsprofiler og patientmål i stedet for en one-size-fits-all tilgang.
Personalisering af behandling: mere end huddybde
Klinikere understreger, at valg af behandling er en individualiseret proces. Ingen enkelt faktor bestemmer den ideelle terapi: sygdomsgrad, komorbide tilstande (som astma eller allergisk rhinitis), tidligere behandlingsreaktioner, sikkerhedsmæssige bekymringer og patientpræferencer betyder alt.
Fordi atopisk dermatitis er en multifacetteret sygdom—der påvirker søvn, humør, social funktion og mere—fanger visuel inspektion alene ikke hele billedet. At lytte til patienter om kløens sværhedsgrad, indvirkning på dagliglivet og deres tolerance for visse risici er essentielt for at vælge den mest passende mulighed.
I praksis betyder det, at mange praktikere bruger en model for delt beslutningstagning: klinikere præsenterer de rimelige muligheder, forklarer fordele og risici, og derefter samarbejder de med patienten om at vælge en vej frem.
Bevidsthed om systemisk inflammation og komorbiditet
Moderne syn på AD anerkender i stigende grad, at det er en systemisk inflammatorisk lidelse snarere end en rent hudbegrænset tilstand. Dette perspektiv hjælper med at forklare, hvorfor personer med AD ofte har relaterede atopiske eller inflammatoriske tilstande.
Fordi nogle målrettede terapier påvirker immunveje, der er fælles for flere sygdomme, kan deres brug påvirke, positivt eller negativt, samtidig eksisterende tilstande. Som et resultat tager klinikere oftere komorbiditetsprofiler med i behandlingsvalg end før (Kilde: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Eksperter bemærker også behovet for kliniske forsøg, der prospektivt vurderer, hvordan behandlingerne præsterer hos patienter med almindelige komorbiditeter, for bedre at afspejle den virkelige praksis og vejlede klinikere i at vælge terapier, der forbedrer den samlede sundhed, ikke kun hudsymptomer.
“Vi har brug for forsøg, der eksplicit inkluderer vurderinger af komorbiditet, så vi kan begynde at opdele terapier i henhold til bredere patientbehov,” observerede en specialist.
Fokus på kronisk håndeksem og pædiatrisk pleje
To områder, der får mere opmærksomhed, er kronisk håndeksem (CHE) og pædiatrisk atopisk dermatitis, som historisk set har været udfordrende at behandle og nogle gange undererkendt i voksne klinikker.
CHE er ofte invaliderende på grund af smerte, revner og indgreb i arbejde eller pleje. Nyligt godkendte topiske midler, der specifikt er undersøgt for håndsygdom—mest bemærkelsesværdigt godkendelsen af topisk delgocitinib til kronisk håndeksem—giver klinikere nye, evidensbaserede muligheder for dette område (Kilde: LEO Pharma pressemeddelelse).
Mange systemiske og topiske AD-terapier inkluderer også håndspecifikke eller håndnære data i deres udviklingsprogrammer, hvilket hjælper klinikere med at træffe mere informerede valg, når hænderne er det primære problem.
For børn har det terapeutiske landskab også udvidet sig. Flere systemiske terapier og flere topiske midler er blevet undersøgt og godkendt til yngre aldersgrupper i de seneste år, hvilket giver mere fleksibilitet til at tilpasse regimer til pædiatriske patienter, herunder dem med moderat til svær sygdom eller betydelig indvirkning på livskvaliteten (Kilde: Incyte; Regeneron; Pfizer pressemeddelelser).
Praktiske overvejelser: sikkerhed, overvågning og patientpræferencer
Valg af et målrettet middel kræver en balance mellem forventede fordele og behovet for sikkerhedsovervågning samt patientens komfort med potentielle bivirkninger. For eksempel kan JAK-hæmmere kræve forskellige baseline-screeninger og periodiske laboratorietests sammenlignet med biologiske monoklonale antistoffer, og patienter bør informeres om disse praktiske forskelle.
Topiske ikke-steroide midler kan være attraktive for langvarig lokal kontrol, når sikkerhed og bekvemmelighed er prioriteter, mens systemiske midler forbliver vigtige for omfattende eller refraktær sygdom. Alle disse valg bør træffes i konteksten af en åben dialog om mål, risici, overvågning og omkostninger eller adgangsproblemer.
Ser fremad: genetik, biomarkører og smartere forsøg
Nye værktøjer—som genetiske tests og molekylære biomarkører—sigter mod at forfine behandlingsvalget mellem biologiske midler og orale JAK-hæmmere, men deres rutinemæssige kliniske nytte er stadig under diskussion.
Klinikere er håbefulde om, at når biomarkører valideres og inkorporeres i forsøg, vil de hjælpe med at forudsige, hvem der vil reagere bedst på en given terapi, reducere den tid, der bruges på ineffektive behandlinger, og yderligere personalisere plejen.
Imens presser feltet på for kliniske forsøg designet til at afspejle kompleksiteten af typiske patienter—herunder komorbiditeter og virkelige behandlingsrækkefølger—så evidensen bedre matcher den daglige praksis.
Konklusion
Den nuværende æra af AD-pleje er præget af præcision og personalisering: klinikere har nu en rigere værktøjskasse, der inkluderer målrettede biologiske midler, orale JAK-hæmmere og nye topiske ikke-steroide midler, hvilket muliggør mere skræddersyede behandlingsplaner, der er tilpasset patienternes behov og sikkerhedsovervejelser.
Delt beslutningstagning, bevidsthed om systemisk inflammation og komorbiditeter samt omhyggelig valg og sekventering af terapier er nøglen til at opnå de bedste resultater for personer, der lever med atopisk dermatitis.
Kilder
- American Academy of Dermatology Association, Atopic Dermatitis Guidelines (retningslinjedokumenter og kliniske ressourcer).
- Regeneron Pharmaceuticals og Sanofi pressematerialer om dupilumab (FDA-godkendelse og klinisk programinformation).
- Pfizer pressemeddelelse og ordinationsinformation for abrocitinib (CIBINQO).
- AbbVie pressemeddelelse og produktinformation for upadacitinib (RINVOQ) ved atopisk dermatitis.
- Incyte Corporation pressemeddelelser og FDA-kommunikation vedrørende topisk ruxolitinib (Opzelura).
- LEO Pharma pressemeddelelser relateret til tralokinumab og topisk delgocitinib udviklinger og godkendelser.
- Eli Lilly pressemeddelelser og regulatoriske kommunikationer om lebrikizumab.
- Virksomhedens pressematerialer og kliniske forsøgsoversigter for topiske midler som tapinarof og roflumilast (Dermavant/Arcutis og andre udviklerressourcer).
