Uued tipptasemel ravimeetodid muudavad atoopilise dermatiidi hooldust 2026. aastal.
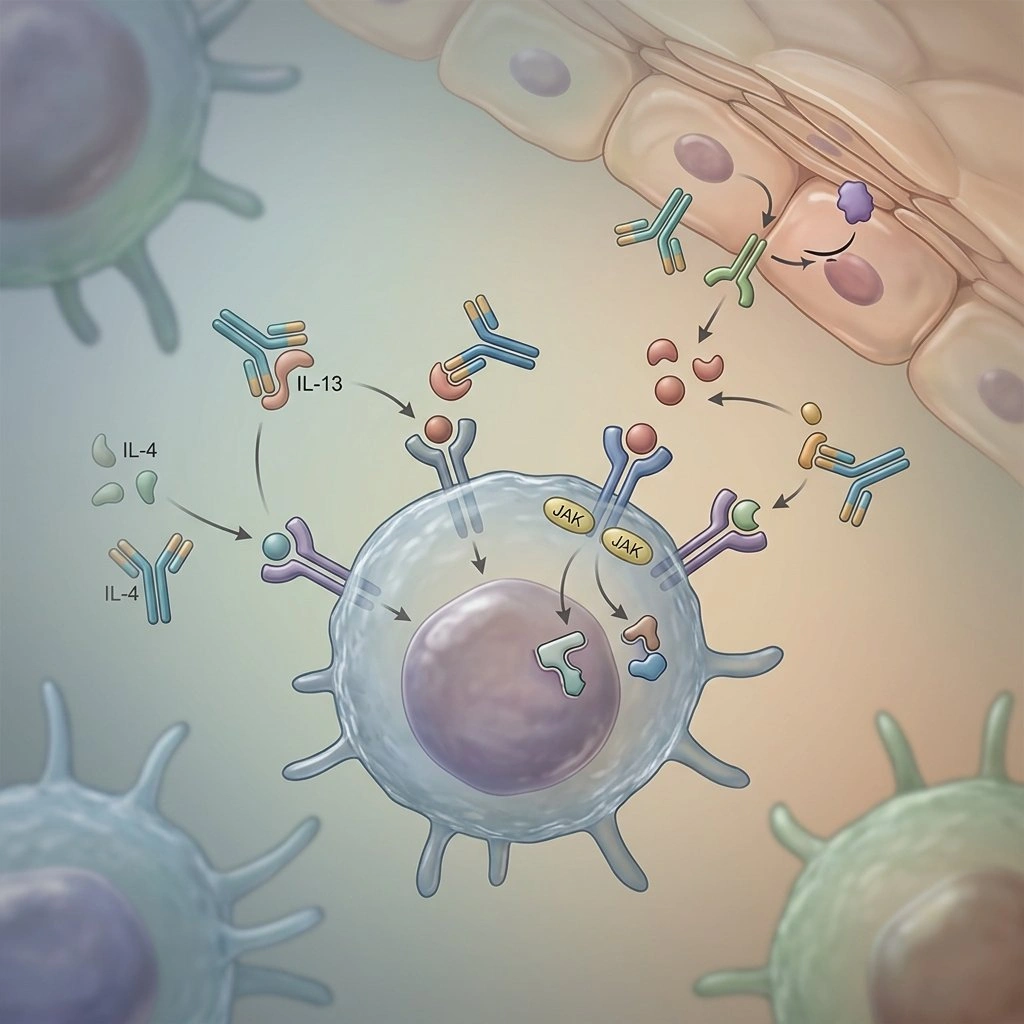
Uus ajastu: sihitud ravimid muudavad atoopilise dermatiidi ravi
Viimastel aastatel on atoopilise dermatiidi (AD) ravi liikunud laiaulatuslikest põletikuvastastest ravimitest sihitud valikute suunas, mis hõlmavad bioloogilisi monokloonilisi antikehi, suukaudseid Janus kinaasi (JAK) inhibiitoreid ja uusi mitte-steroidseid paikseid aineid.
Need uuemad valikud ei ole lihtsalt lisavalikud; need on ümber kujundanud reaalsed otsuste tegemise protsessid kliinikutes. Arstid kaaluvad nüüd sihitud ainete varasemat kasutamist, mitte ei jäta neid viimase ravina, kuna paljud neist ravimitest pakuvad püsivat haiguse kontrolli mehhanismide kaudu, mis on suunatud patsiendi ekseemi spetsiifilisele bioloogiale (Allikas: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Kuidas spetsialistid mõtlevad ravijärjestusele
Viimase erialakonverentsi juhtivad arstid kirjeldasid selget muutust praktikas: sihitud ravimid on üha enam pikaajalise ravi aluseks, samas kui traditsioonilisi aineid—nagu paiksed kortikosteroidid ja paiksed kalcineuriini inhibiitorid—kasutatakse sageli lühiajaliste sildadena või fokaalsete ägenemiste korral.
See muutus peegeldab kasvavat usaldust sihitud ravimite ohutuse ja püsivate vastuste osas ning soovi vältida võimalikult kaua kestvat, mittespetsiifilist immuunsupressiooni (Allikas: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Mida tähendab “sihitud” igapäevases hoolduses
Kui dermatoloogid räägivad “sihitud” ravimitest, siis nad mõtlevad teraapiaid, mis katkestavad määratletud immuunsüsteemi tee, mis on tuntud AD sümptomite põhjustajana—seega, selle asemel, et immuunsüsteemi aktiivsust laialdaselt vähendada, blokeerivad need ravimid spetsiifilisi tsütokiine või signaalimolekule. See võib paljudele patsientidele tähendada paremat sügeluse kontrolli, paremat und ja selgemat nahka.
Praktikat muutvad näited hõlmavad anti-IL-4/IL-13 monokloonilist antikeha dupilumab ja suukaudseid JAK inhibiitoreid, nagu abrocitinib ja upadacitinib, mis on kõik muutunud tavapärasteks valikuteks mõõduka kuni raske haiguse korral (Allikas: Regeneron Pharmaceuticals; Pfizer; AbbVie pressiteated).
Laienev terapeutiline maastik: mis on praegu saadaval
Heakskiidetud ja uurimisalaste valikute valik on kiiresti laienenud, pakkudes arstidele ja patsientidele rohkem võimalusi ravivõimaluste kohandamiseks individuaalsetele vajadustele.
Paiksed, mitte-steroidsed ravimid—nagu tapinarof, paikne ruxolitinib ja roflumilast—on andnud arstidele alternatiive pikaajaliseks paikseks kontrolliks, eriti kui soovitakse vähendada steroidide kasutamist (Allikas: Dermavant/Incyte/Arcutis pressiteated).
Systemaatilisel poolel pakuvad suukaudsed JAK inhibiitorid (näiteks abrocitinib ja upadacitinib) ja mitmed bioloogilised monokloonilised antikehad (sealhulgas dupilumab, tralokinumab, lebrikizumab ja nemolizumab) väga sihitud valikuid patsientidele, kellel on laialdane, ravimiresistentne või raske haigus (Allikas: Pfizer; AbbVie; Regeneron; LEO Pharma; Eli Lilly; ettevõtte pressiteated).
Liialt vähestest valikutest liiga paljude valikute juurde
Kuigi rohkem ravimeid on hea uudis, on see muutnud kliinilist väljakutset: arstid seisavad silmitsi keeruliste otsustega, millist ravi alustada, millal vahetada ja kuidas ravimeid järjestada parima pikaajalise tulemuse saavutamiseks.
See keerukus nõuab haiguse omaduste, ohutuse ja patsiendi eesmärkide hoolikat hindamist, mitte ühtset lähenemist.
Ravi isikupärastamine: rohkem kui nahapind
Arstid rõhutavad, et ravivaliku tegemine on individuaalne protsess. Ükski tegur ei määra ideaalset ravi: haiguse raskusaste, kaasnevad haigused (nagu astma või allergiline nohu), varasemad ravivastused, ohutuse mured ja patsiendi eelistused on kõik olulised.
Kuna atoopiline dermatiit on mitmekülgne haigus—mõjutades und, meeleolu, sotsiaalset toimimist ja palju muud—ei piisa visuaalsest kontrollist kogu pildi tabamiseks. Patsientide kuulamine sügeluse raskuse, igapäevaelu mõjude ja nende taluvuse osas teatud riskide suhtes on hädavajalik kõige sobivama valiku tegemiseks.
Praktikas tähendab see, et paljud praktikandid kasutavad jagatud otsuste tegemise mudelit: arstid esitavad mõistlikud valikud, selgitavad eeliseid ja riske ning seejärel teevad koostööd patsiendiga, et valida edasine tee.
Systemaatiline põletik ja kaasuvate haiguste teadlikkus
Kaasaegsed vaated AD-le tunnustavad seda üha enam süsteemse põletikulise häirena, mitte lihtsalt nahaga piirduva seisundina. See perspektiiv aitab selgitada, miks AD-ga inimestel on sageli seotud atoopilised või põletikulised seisundid.
Kuna mõned sihitud ravimid mõjutavad immuunsüsteemi teid, mis on tavalised mitmete haiguste puhul, võib nende kasutamine positiivselt või negatiivselt mõjutada kaasnevaid seisundeid. Seetõttu arvestavad arstid üha enam kaasuvate haiguste profiile ravivalikutes (Allikas: American Academy of Dermatology, Atopic Dermatitis Guidelines).
Eksperdid märgivad ka vajadust kliiniliste uuringute järele, mis hindavad prospektiivselt, kuidas ravimid toimivad patsientidel, kellel on tavalised kaasnevad haigused, et paremini peegeldada reaalseid praktikaid ja suunata arste valima ravimeid, mis parandavad üldist tervist, mitte ainult nahasümptomeid.
„Me vajame uuringuid, mis sisaldavad selgelt kaasuvate haiguste hindamisi, et saaksime hakata ravimeid eristama laiemate patsiendi vajaduste järgi,“ märkis üks spetsialist.
Fookuses krooniline käte ekseem ja laste ravi
Kaks valdkonda, mis saavad rohkem tähelepanu, on krooniline käte ekseem (CHE) ja laste atoopiline dermatiit, mis on mõlemad ajalooliselt olnud ravimise osas keerulised ja mõnikord alahinnatud täiskasvanute kliinikutes.
CHE on sageli puuet tekitav valu, pragunemise ja töö või hooldamise häirimise tõttu. Hiljuti heakskiidetud paiksed ained, mis on spetsiaalselt uuritud käte haiguse jaoks—eriti paikse delgocitinibi heakskiit kroonilise käte ekseemi jaoks—annavad arstidele uusi, tõenduspõhiseid valikuid selle piirkonna jaoks (Allikas: LEO Pharma pressiteade).
Paljud süsteemsed ja paiksed AD ravimid sisaldavad ka käte spetsiifilisi või kätega külgnevaid andmeid oma arendusprogrammides, mis aitab arstidel teha teadlikumaid valikuid, kui käed on peamine probleem.
Laste jaoks on terapeutiline maastik samuti laienenud. Viimastel aastatel on mitmeid süsteemseid ravimeid ja mitmeid paikseid aineid uuritud ja heaks kiidetud nooremate vanuserühmade jaoks, pakkudes rohkem paindlikkust raviskeemide kohandamiseks laste patsientide jaoks, sealhulgas mõõduka kuni raske haiguse või elukvaliteedi olulise mõju korral (Allikas: Incyte; Regeneron; Pfizer pressiteated).
Praktilised kaalutlused: ohutus, jälgimine ja patsiendi eelistused
Sihitud aine valimine nõuab oodatavate eeliste tasakaalustamist ohutuse jälgimise vajaduste ja patsiendi mugavusega võimalike kõrvaltoimete osas. Näiteks JAK inhibiitorid võivad vajada erinevat baasskriiningut ja perioodilisi laboratoorseid analüüse võrreldes bioloogiliste monoklooniliste antikehadega, ning patsiente tuleks nende praktiliste erinevuste osas nõustada.
Paiksed mitte-steroidsed ained võivad olla atraktiivsed pikaajaliseks kohalikuks kontrolliks, kui ohutus ja mugavus on prioriteediks, samas kui süsteemsed ained jäävad olulisteks ulatusliku või ravimiresistentse haiguse korral. Kõik need valikud tuleks teha avatud dialooge arvesse võttes eesmärkide, riskide, jälgimise ja kulude või juurdepääsu küsimuste osas.
Vaadates tulevikku: geneetika, biomarkerid ja nutikam uuringud
Uued tööriistad—nagu geneetilised testid ja molekulaarsed biomarkerid—püüavad täpsustada ravivalikut bioloogiliste ja suukaudsete JAK inhibiitorite vahel, kuid nende rutiinne kliiniline kasulikkus on endiselt arutelu all.
Arstid loodavad, et kui biomarkerid valideeritakse ja kaasatakse uuringutesse, aitavad need ennustada, kes reageerib kõige paremini antud ravile, vähendavad aega, mis kulub ebaefektiivsetele ravidele, ja isikupärastavad hooldust veelgi.
Vahepeal surub valdkond kliiniliste uuringute poole, mis on kavandatud peegeldama tüüpiliste patsientide keerukust—sealhulgas kaasnevaid haigusi ja reaalse maailma ravijärjestust—nii, et tõendid vastaksid paremini igapäevasele praktikale.
Oluline kokkuvõte
Praegune AD hoolduse ajastu on iseloomustatud täpsuse ja isikupärastamisega: arstidel on nüüd rikkam tööriistakast, mis sisaldab sihitud bioloogilisi ravimeid, suukaudseid JAK inhibiitoreid ja uusi paikseid mitte-steroidseid aineid, võimaldades rohkem kohandatud raviplaane, mis vastavad patsiendi vajadustele ja ohutuse kaalutlustele.
Jagatud otsuste tegemine, teadlikkus süsteemsest põletikust ja kaasnevatest haigustest ning hoolikas ravimite valik ja järjestamine on võtmetähtsusega parimate tulemuste saavutamiseks atoopilise dermatiidiga inimestele.
Allikad
- American Academy of Dermatology Association, Atopic Dermatitis Guidelines (suunised ja kliinilised ressursid).
- Regeneron Pharmaceuticals ja Sanofi pressimaterjalid dupilumab (FDA heakskiit ja kliinilise programmi teave).
- Pfizer pressiteade ja retseptiravimi teave abrocitinib (CIBINQO) kohta.
- AbbVie pressiteade ja tooteinfo upadacitinib (RINVOQ) kohta atoopilise dermatiidi puhul.
- Incyte Corporation pressiteated ja FDA teated seoses paikse ruxolitinib (Opzelura) kasutamisega.
- LEO Pharma pressiteated, mis on seotud tralokinumab ja paikse delgocitinibi arenduste ja heakskiitudega.
- Eli Lilly pressiteated ja regulatiivsed teated lebrikizumab kohta.
- Ettevõtte pressimaterjalid ja kliiniliste uuringute kokkuvõtted paiksete ainete, nagu tapinarof ja roflumilast (Dermavant/Arcutis ja muud arendaja ressursid).
