Des traitements de pointe transforment les soins de la dermatite atopique en 2026.
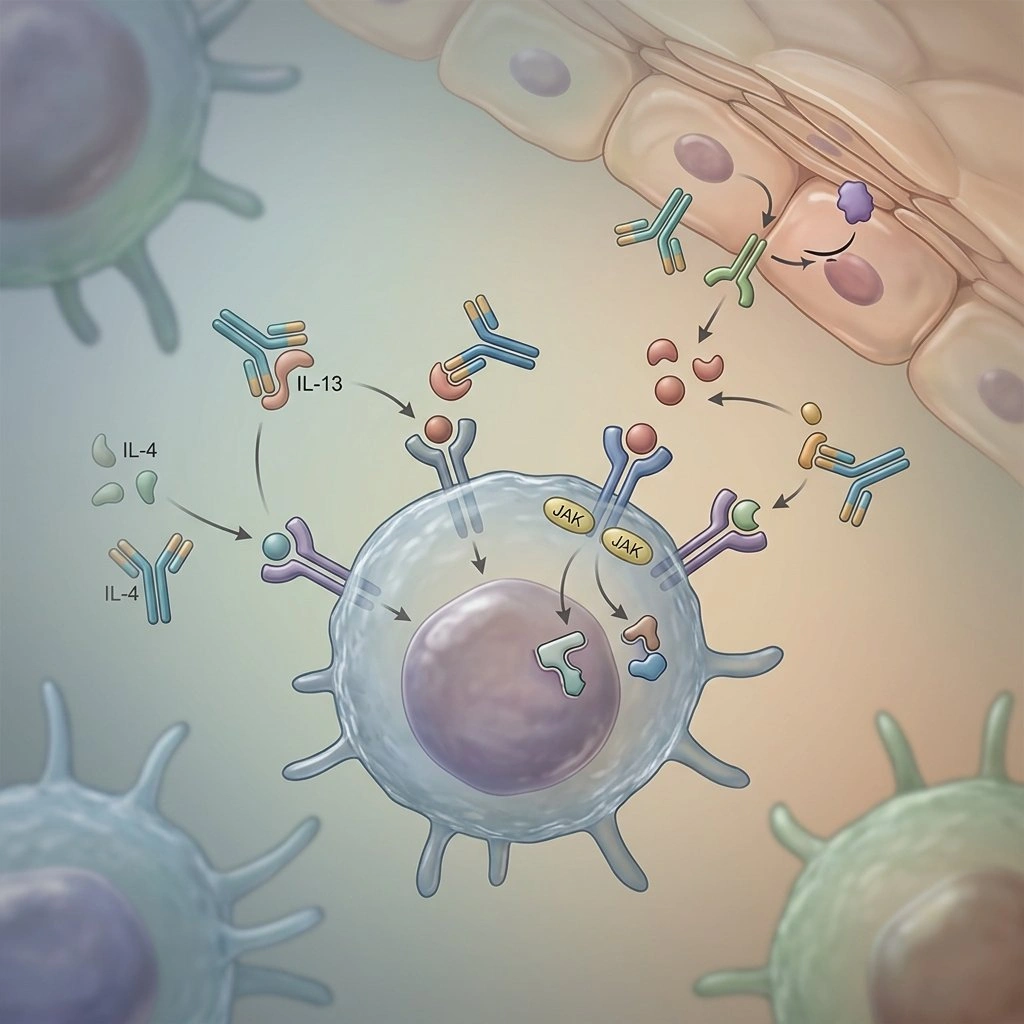
Une nouvelle ère : les médicaments ciblés changent notre façon de traiter la dermatite atopique
Au cours des dernières années, le traitement de la dermatite atopique (DA) est passé d’une boîte à outils dominée par des médicaments anti-inflammatoires larges à une boîte qui inclut des options hautement ciblées : des anticorps monoclonaux biologiques, des inhibiteurs de Janus kinase (JAK) oraux et de nouveaux agents topiques non stéroïdiens.
Ces nouvelles options ne sont pas seulement des choix supplémentaires ; elles ont remodelé la prise de décision dans les cliniques. Les cliniciens envisagent désormais d’utiliser plus tôt des agents ciblés au lieu de les réserver comme traitements de dernier recours, car beaucoup de ces médicaments offrent un contrôle durable de la maladie avec des mécanismes visant la biologie spécifique qui sous-tend l’eczéma d’un patient (Source : American Academy of Dermatology, Atopic Dermatitis Guidelines).
Comment les spécialistes réfléchissent à la séquence de traitement
Des cliniciens de premier plan lors d’une récente conférence spécialisée ont décrit un changement clair dans la pratique : les thérapies ciblées deviennent de plus en plus la colonne vertébrale de la gestion à long terme, tandis que les agents traditionnels—comme les corticostéroïdes topiques et les inhibiteurs de calcineurine topiques—sont souvent utilisés comme des solutions temporaires ou pour des poussées localisées.
Ce changement reflète une confiance croissante dans les profils de sécurité et les réponses durables des médicaments ciblés, ainsi qu’un désir d’éviter une immunosuppression prolongée et non spécifique lorsque cela est possible (Source : American Academy of Dermatology, Atopic Dermatitis Guidelines).
Ce que signifie « ciblé » dans les soins quotidiens
Lorsque les dermatologues parlent de « ciblé », ils font référence à des thérapies qui interrompent une voie immunitaire définie connue pour provoquer des symptômes de DA—plutôt que de réduire largement l’activité immunitaire, ces médicaments bloquent des cytokines ou des molécules de signalisation spécifiques. Cela peut se traduire par un meilleur contrôle des démangeaisons, un sommeil amélioré et une peau plus claire pour de nombreux patients.
Des exemples qui ont modifié la pratique incluent l’anticorps monoclonal anti-IL-4/IL-13 dupilumab, et des inhibiteurs de JAK oraux tels que abrocitinib et upadacitinib, qui sont devenus des options courantes pour les maladies modérées à sévères (Source : Regeneron Pharmaceuticals ; Pfizer ; AbbVie communiqués de presse).
Un paysage thérapeutique en expansion : ce qui est disponible maintenant
La gamme d’options approuvées et en cours d’investigation s’est rapidement élargie, offrant aux cliniciens et aux patients davantage de moyens d’adapter le traitement aux besoins individuels.
Les médicaments topiques non stéroïdiens—comme tapinarof, ruxolitinib topique, et roflumilast—ont donné aux cliniciens des alternatives pour un contrôle topique à long terme, en particulier lorsque la minimisation de l’exposition aux stéroïdes est souhaitée (Source : Dermavant/Incyte/Arcutis communiqués de presse).
Du côté systémique, les inhibiteurs de JAK oraux (par exemple, abrocitinib et upadacitinib) et plusieurs anticorps monoclonaux biologiques (y compris dupilumab, tralokinumab, lebrikizumab, et nemolizumab) offrent des options hautement ciblées pour les patients atteints de maladies étendues, réfractaires ou sévères (Source : Pfizer ; AbbVie ; Regeneron ; LEO Pharma ; Eli Lilly ; communiqués de presse des entreprises).
De trop peu d’options à trop de choix
Bien que disposer de plus de traitements soit une bonne nouvelle, cela a modifié le défi clinique : les médecins sont désormais confrontés à des décisions complexes concernant le choix de la thérapie à commencer, le moment de changer, et comment séquencer les traitements pour obtenir le meilleur résultat à long terme.
Cette complexité nécessite une évaluation minutieuse des caractéristiques de la maladie, des profils de sécurité et des objectifs des patients plutôt qu’une approche universelle.
Personnaliser le traitement : plus qu’une question de peau
Les cliniciens soulignent que la sélection du traitement est un processus individualisé. Aucun facteur unique ne détermine la thérapie idéale : la sévérité de la maladie, les conditions comorbides (comme l’asthme ou la rhinite allergique), les réponses aux traitements antérieurs, les préoccupations de sécurité et les préférences des patients sont tous importants.
Étant donné que la dermatite atopique est une maladie multifacette—affectant le sommeil, l’humeur, le fonctionnement social, et plus encore—une simple inspection visuelle ne capture pas l’ensemble du tableau. Écouter les patients sur la gravité des démangeaisons, l’impact sur la vie quotidienne, et leur tolérance à certains risques est essentiel pour choisir l’option la plus appropriée.
Dans la pratique, cela signifie que de nombreux praticiens utilisent un modèle de prise de décision partagée : les cliniciens présentent les options raisonnables, expliquent les avantages et les risques, puis s’associent au patient pour choisir une voie à suivre.
Connaissance de l’inflammation systémique et des comorbidités
Les vues modernes de la DA reconnaissent de plus en plus qu’il s’agit d’un trouble inflammatoire systémique plutôt que d’une condition purement limitée à la peau. Cette perspective aide à expliquer pourquoi les personnes atteintes de DA ont souvent des conditions atopiques ou inflammatoires associées.
Comme certaines thérapies ciblées affectent des voies immunitaires communes à plusieurs maladies, leur utilisation peut influencer, positivement ou négativement, les conditions coexistantes. En conséquence, les cliniciens prennent de plus en plus en compte les profils de comorbidité dans leurs choix de traitement (Source : American Academy of Dermatology, Atopic Dermatitis Guidelines).
Les experts notent également la nécessité d’essais cliniques qui évaluent prospectivement comment les traitements fonctionnent chez les patients présentant des comorbidités courantes, afin de mieux refléter la pratique réelle et d’aider les cliniciens à sélectionner des thérapies qui améliorent la santé globale, et pas seulement les symptômes cutanés.
« Nous avons besoin d’essais qui incluent explicitement des évaluations de comorbidité afin que nous puissions commencer à différencier les thérapies en fonction des besoins plus larges des patients », a observé un spécialiste.
Zoom sur l’eczéma des mains chronique et les soins pédiatriques
Deux domaines qui reçoivent plus d’attention sont l’eczéma des mains chronique (EMC) et la dermatite atopique pédiatrique, tous deux historiquement difficiles à traiter et parfois sous-reconnus dans les cliniques pour adultes.
L’EMC est souvent invalidant en raison de la douleur, des fissures, et de l’interférence avec le travail ou les soins. Des agents topiques récemment approuvés spécifiquement étudiés pour la maladie des mains—notamment l’approbation du delgocitinib topique pour l’eczéma des mains chronique—offrent aux cliniciens de nouvelles options basées sur des preuves pour ce site (Source : LEO Pharma communiqué de presse).
De nombreuses thérapies systémiques et topiques pour la DA incluent également des données spécifiques aux mains ou adjacentes aux mains dans leurs programmes de développement, ce qui aide les cliniciens à faire des choix plus éclairés lorsque les mains sont le principal problème.
Pour les enfants, le paysage thérapeutique s’est également élargi. Plusieurs thérapies systémiques et de multiples agents topiques ont été étudiés et approuvés pour les groupes d’âge plus jeunes ces dernières années, offrant plus de flexibilité pour adapter les régimes pour les patients pédiatriques, y compris ceux atteints de maladies modérées à sévères ou ayant un impact significatif sur la qualité de vie (Source : Incyte ; Regeneron ; Pfizer communiqués de presse).
Considérations pratiques : sécurité, suivi et préférences des patients
Choisir un agent ciblé nécessite d’équilibrer les bénéfices attendus avec les besoins de suivi de sécurité et le confort du patient face aux effets secondaires potentiels. Par exemple, les inhibiteurs de JAK peuvent nécessiter un dépistage de base différent et des analyses périodiques par rapport aux anticorps monoclonaux biologiques, et les patients doivent être informés de ces différences pratiques.
Les agents topiques non stéroïdiens peuvent être attrayants pour un contrôle local à long terme lorsque la sécurité et la commodité sont des priorités, tandis que les agents systémiques restent importants pour les maladies étendues ou réfractaires. Tous ces choix doivent être faits dans le cadre d’un dialogue ouvert sur les objectifs, les risques, le suivi, et les questions de coût ou d’accès.
À l’avenir : génétique, biomarqueurs et essais plus intelligents
Les outils émergents—comme les tests génétiques et les biomarqueurs moléculaires—visent à affiner la sélection des traitements entre les biologiques et les inhibiteurs de JAK oraux, mais leur utilité clinique de routine est encore en discussion.
Les cliniciens espèrent qu’à mesure que les biomarqueurs seront validés et intégrés dans les essais, ils aideront à prédire qui répondra le mieux à une thérapie donnée, à réduire le temps passé sur des traitements inefficaces, et à personnaliser davantage les soins.
En attendant, le domaine pousse pour des essais cliniques conçus pour refléter la complexité des patients typiques—y compris les comorbidités et la séquence de traitement dans la vie réelle—afin que les preuves correspondent mieux à la pratique quotidienne.
Conclusion
L’ère actuelle des soins pour la DA est marquée par la précision et la personnalisation : les cliniciens disposent désormais d’une boîte à outils plus riche qui inclut des biologiques ciblés, des inhibiteurs de JAK oraux, et de nouveaux agents topiques non stéroïdiens, permettant des plans de traitement plus adaptés aux besoins des patients et aux considérations de sécurité.
La prise de décision partagée, la prise de conscience de l’inflammation systémique et des comorbidités, ainsi que la sélection réfléchie et la séquence des thérapies sont essentielles pour obtenir les meilleurs résultats pour les personnes vivant avec une dermatite atopique.
Sources
- American Academy of Dermatology Association, Atopic Dermatitis Guidelines (documents de directives et ressources cliniques).
- Regeneron Pharmaceuticals et Sanofi documents de presse sur dupilumab (approbation par la FDA et informations sur le programme clinique).
- Communiqué de presse de Pfizer et informations de prescription pour abrocitinib (CIBINQO).
- Communiqué de presse d’AbbVie et informations sur le produit pour upadacitinib (RINVOQ) dans la dermatite atopique.
- Communiqués de presse de la société Incyte et communications de la FDA concernant ruxolitinib topique (Opzelura).
- Communiqués de presse de LEO Pharma liés aux développements et approbations de tralokinumab et delgocitinib topique.
- Communiqués de presse d’Eli Lilly et communications réglementaires sur lebrikizumab.
- Documents de presse de la société et résumés d’essais cliniques pour des agents topiques tels que tapinarof et roflumilast (Dermavant/Arcutis et autres ressources des développeurs).
